

第Ⅲ相臨床試験 ②(単剤長期投与試験)
1試験概要
デザイン |
非盲検試験(長期投与試験) |
|---|---|
| 目的 | 食事療法・運動療法にて血糖コントロール不十分な2型糖尿病患者を対象に、ルセフィを52週間長期投与した際の安全性および有効性を検討する。 |
| 対象 | 食事・運動療法にて血糖コントロール不十分な2型糖尿病患者299例
|
| 方法 |
ルセフィ2.5mgを1日1回、朝食前に52週間経口投与した。ただし、増量基準※を満たした場合は、投与24週にルセフィ5mg1 日1 回への増量を可とした。 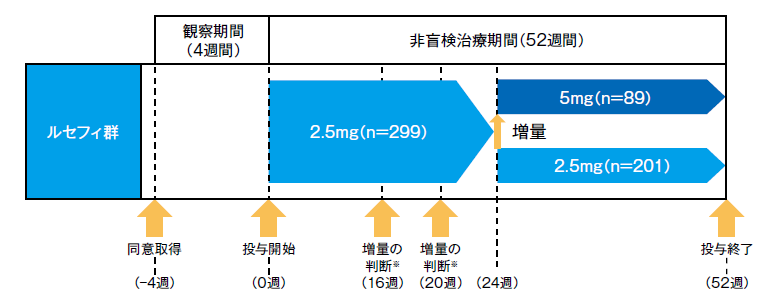
|
| 評価方法 | 治療開始時、2 週、4 週、以後4 週ごとに52 週までHbA1c、空腹時血糖値(朝食前)、体重を測定した。 |
| 評価項目 |
安全性評価項目:有害事象(臨床検査値、バイタルサイン、12誘導心電図を含む)の内容および発現頻度 有効性評価項目:HbA1c、空腹時血糖値、グリコアルブミン、体重、空腹時インスリン、血中CPR、インタクトプロインスリン、HOMA-R、HOMA-β (HbA1c はNGSP値で表記) |
| 解析計画 | 有効性の解析対象はFASとした。各評価時期の治療期開始時(ベースライン)からの変化量を用いて信頼区間を算出し、1標本t検定を行った。 |
- 社内資料(臨床試験HbA1c[NGSP値]再解析結果)
- 承認時評価資料(単剤長期投与試験)
- Seino Y et al.: Endocr J. 2015; 62: 593-603.
- [利益相反]本試験は、大正製薬株式会社の支援によって行われました。
生方路人、坂井荘一、寒川能成は、大正製薬株式会社の社員です。
第Ⅲ相臨床試験 ②(単剤長期投与試験)
2HbA1cの改善効果
ベースラインからのHbA1c変化量は、投与52週で−0.50%であり、ベースラインに比べて有意な低下が認められた。ルセフィ2.5mg群※において、投与2週からHbA1cの有意な低下が認められ、52週まで維持された。
■投与52週におけるベースラインからのHbA1c変化量およびHbA1c変化量の推移
投与52週におけるベースラインからのHbA1c変化量
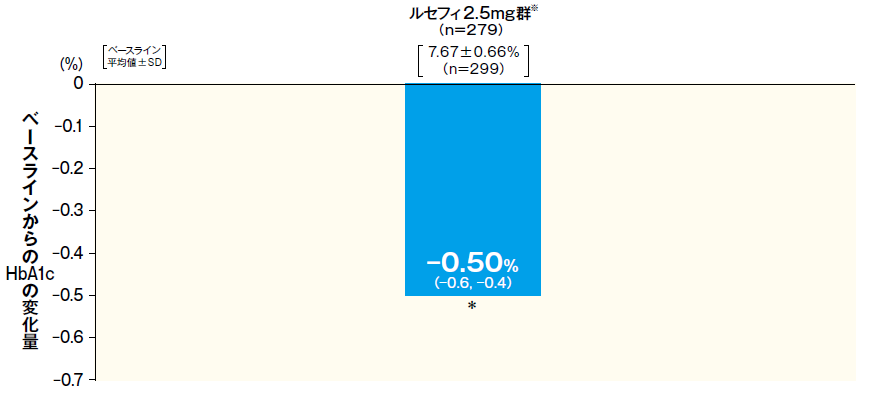
- FAS 平均値(95%CI)
- *:p < 0. 001(vs. ベースライン)、1標本t検定
HbA1c変化量の推移
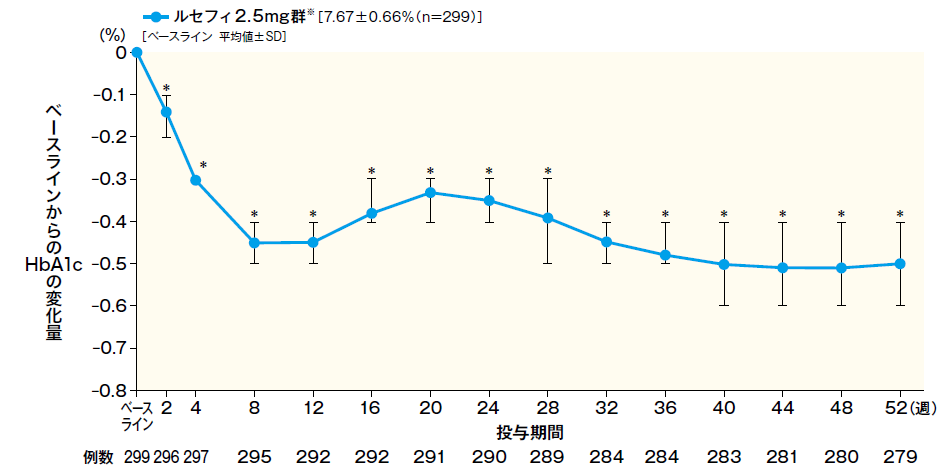
- FAS 平均値(95%CI)
- *:p < 0. 001(vs. ベースライン)、1標本t検定
- ※投与24週にルセフィ5mgへ増量した例を含む。
第Ⅲ相臨床試験 ②(単剤長期投与試験)
3空腹時血糖値の改善効果
ルセフィ2.5mg群※のベースラインからの空腹時血糖値の変化量は、投与24週で−11.3mg/dL、52週においては−16.3mg/dLであり、いずれもベースラインに比べて有意な低下が認められた。
■ベースラインからの空腹時血糖値変化量の推移
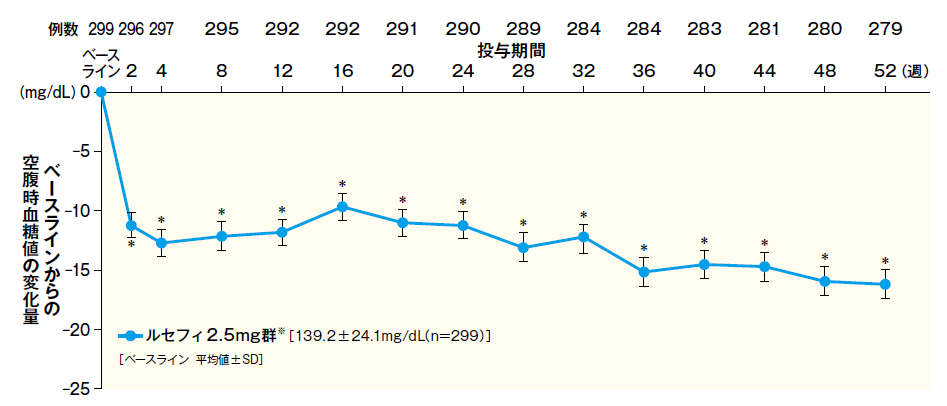
- FAS 平均値 ± SE
- *:p < 0. 001(vs. ベースライン)、1標本t検定
- ※投与24週にルセフィ5mgへ増量した症例を含む。
第Ⅲ相臨床試験 ②(単剤長期投与試験)
4体重に対する影響(参考情報)
ルセフィ2.5mg群※のベースラインからの体重の変化量は、投与24週で−1.91kg、52週においては−2.68kgであり、変化量は以下のように推移した。
■ベースラインからの体重変化量の推移
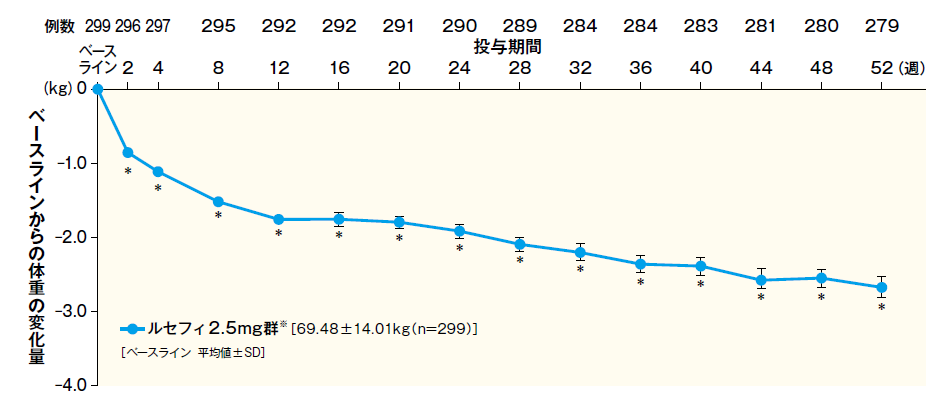
- FAS 平均値 ± SE
- *:p < 0. 001(vs. ベースライン)、1標本t検定
- ※投与24週にルセフィ5mgへ増量した症例を含む。
- 8.重要な基本的注意(抜粋)
- 8.7 本剤投与による体重減少が報告されているため、過度の体重減少に注意すること。
第Ⅲ相臨床試験 ②(単剤長期投与試験)
5安全性
本試験のルセフィ2.5mg群※における副作用の発現率は16.7%(50/299例)で、主な副作用は、便秘9例(3.0%)、頻尿9例(3.0%)、口渇5例(1.7%)、尿中 β2ミクログロブリン増加4例(1.3%)、低血糖症4例(1.3%)、尿中アルブミン陽性3 例(1.0%)、血中ケトン体増加3 例(1.0%)であった。
また、投与24 週にルセフィ5mgに増量した増量例およびルセフィ2.5mgを52 週投与した非増量例における投与24 週以降の副作用の発現率は、それぞれ2.2%(2/89 例)および5.0%(10/201 例)であった。重篤な副作用は腎細胞癌1 例であった。
投与中止に至った副作用は、発疹および感覚鈍麻(同一症例)1 例、外陰部腟カンジダ症1 例、腎細胞癌1 例であった。なお、本試験において死亡例は認められなかった。
- ※投与24週にルセフィ5mgへ増量した症例を含む。






